Plan du cours :
Contrairement aux modèles expérimentaux classiques (comme le pois ou la drosophile), l’étude de la génétique chez l’Homme présente des défis majeurs. L’impossibilité de réaliser des croisements dirigés pour des raisons éthiques, la longue durée des générations et le faible nombre de descendants obligent les généticiens à utiliser des méthodes indirectes, notamment l’analyse des arbres généalogiques (pédigrées) et l’étude du caryotype. L’objectif de cette leçon est de comprendre comment les caractères héréditaires, qu’ils soient normaux (groupes sanguins) ou liés à des anomalies génétiques, sont transmis aux générations futures.
I — Les difficultés d’étude et certains moyens utilisés en génétique humaine.
1- Les difficultés de l’étude de l’hérédité humaine
L’étude de l’hérédité humaine ne peut pas suivre la démarche expérimentale classique utilisée chez les autres organismes (mouches, pois, souris). Elle se heurte à plusieurs obstacles majeurs :
Difficultés spécifiques à l’espèce humaine :
| Difficulté | Explication | Conséquence |
|---|---|---|
| Impossibilité de croisements orientés | Raisons éthiques et morales | Impossibilité de réaliser des expériences contrôlées |
| Longue durée d’une génération | 20 à 30 ans en moyenne | Étude sur plusieurs générations très longue |
| Faible descendance | Peu d’enfants par couple (2-3 en moyenne) | Impossibilité d’obtenir des résultats statistiques significatifs |
| Nombre élevé de chromosomes | 2n = 46 chromosomes | Grande complexité génétique |
| Absence de lignées pures | Brassage génétique permanent | Difficulté d’identification des génotypes |
Conclusion : Face à ces contraintes, les généticiens humains ont développé des méthodes d’étude indirectes et spécifiques qui permettent néanmoins de comprendre la transmission des caractères héréditaires chez l’Homme.
2- Les outils d’étude de l’hérédité humaine
A- L’arbre généalogique (pedigree)
L’arbre généalogique est une représentation graphique de la transmission d’un ou plusieurs caractères au sein d’une famille sur plusieurs générations.
Conventions de représentation :
| Symbole | Signification |
|---|---|
| Individu de sexe masculin sain | |
| Individu de sexe masculin atteint | |
| Individu de sexe féminin sain | |
| Individu de sexe féminin atteint | |
| Individu porteur sain (hétérozygote) | |
| Union / Mariage | |
| Consanguinité | |
| Descendance | |
| Individu décédé |
Utilité : L’arbre généalogique permet de déterminer le mode de transmission d’un caractère (dominant, récessif, lié au sexe) et d’établir les génotypes probables des individus malgré l’absence de croisements expérimentaux.
B- Le caryotype humain
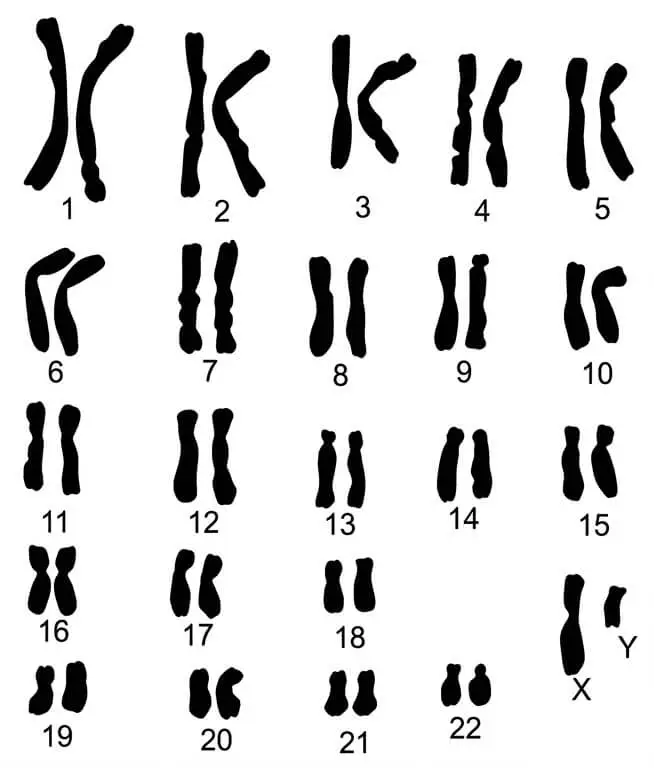
Le caryotype est l’ensemble des chromosomes d’une cellule classés par paires homologues selon leur taille et la position du centromère.
Réalisation du caryotype : Le caryotype est établi à partir de cellules en division (lymphocytes stimulés généralement) puis photographiées en métaphase. Les chromosomes sont ensuite découpés et classés par paires.
Conclusion : Le caryotype permet de diagnostiquer des anomalies chromosomiques (nombre ou structure) et constitue un outil fondamental du diagnostic prénatal.
C- L’analyse de l’ADN par électrophorèse
L’électrophorèse est une technique qui permet de séparer et d’identifier des fragments d’ADN en fonction de leur taille.
Principe de l’électrophorèse : L’ADN, chargé négativement, migre dans un gel d’agarose sous l’effet d’un champ électrique. Les fragments les plus petits migrent plus rapidement que les fragments plus grands.
Étapes de l’analyse :
- Extraction de l’ADN à partir d’un échantillon (sang, salive, cellules)
- Fragmentation de l’ADN par des enzymes de restriction
- Migration électrophorétique dans un gel d’agarose
- Révélation des bandes par coloration ou fluorescence
- Analyse du profil génétique obtenu
Applications en génétique humaine :
| Application | Utilité |
|---|---|
| Diagnostic de maladies génétiques | Détection de mutations (drépanocytose, mucoviscidose) |
| Tests de paternité | Comparaison des profils génétiques |
| Médecine légale | Identification d’individus |
| Dépistage de porteurs sains | Conseil génétique |
II-Transmission de maladies héréditaires liées aux chromosomes sexuels (Maladies gonosomiques)
1-la maladie de Kennedy.
Le document suivant présente l’arbre généalogique d’une famille touchée par la maladie de Kennedy.
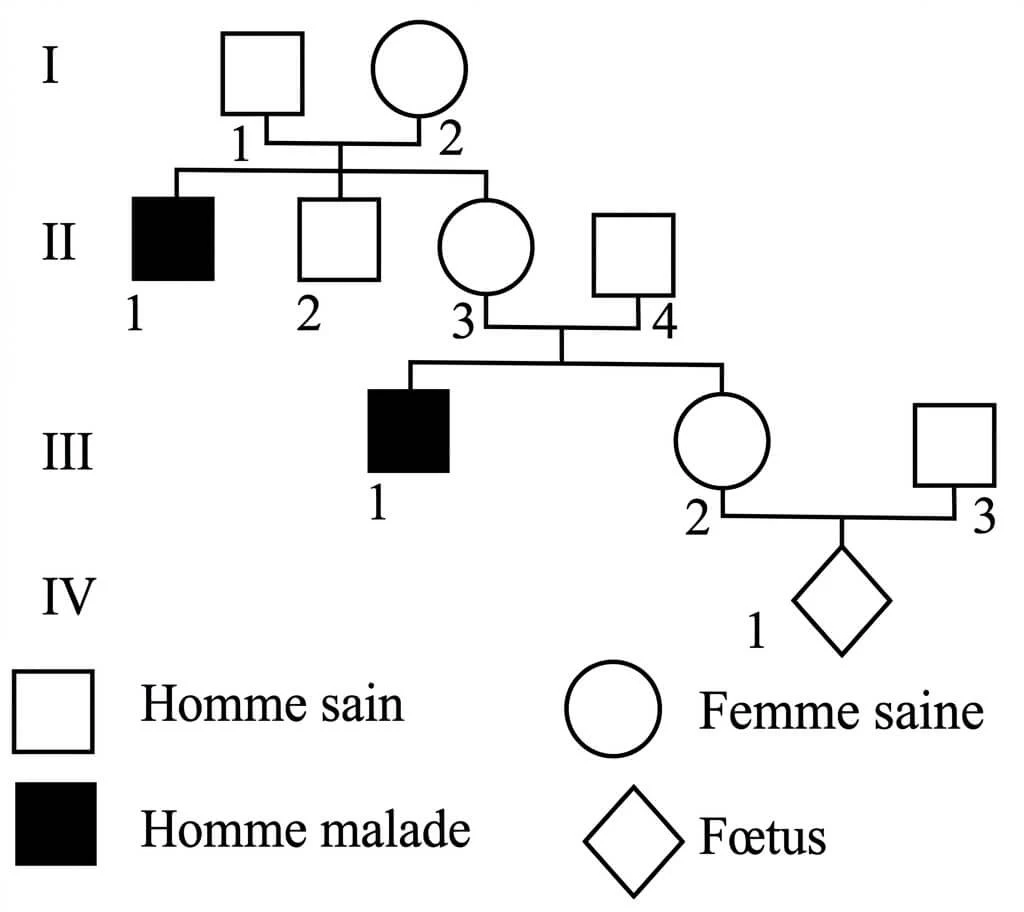
En vous appuyant sur le document :
1. Montrez que l’allèle responsable de la maladie est récessif, puis déterminez les génotypes de I₂, II₁ et III₂.
2. En supposant que III₂ est hétérozygote, calculez la probabilité que le couple (III₂ × III₃) ait un enfant malade, à l’aide d’un échiquier de croisement.
(Symboles à utiliser : N pour l’allèle dominant, n pour l’allèle récessif.)
1.
Les parents I₁ et I₂ (ou II₃ et II₄) sont sains et ont donné naissance à un enfant malade (II₁ ou III₁) → les parents sont hétérozygotes → l’allèle responsable de la maladie est récessif.
La femme I₂ (ou III₂) est saine et a donné naissance à un garçon malade → elle porte l’allèle responsable sans l’exprimer → l’allèle est récessif et porté par le chromosome X.
Génotypes des individus :
I₂ : XNXn— porteuse saine
II₁ : XNY — garçon sain
III₂ : XNXNou XNXn— fille saine (hétérozygote supposée)
b. Probabilité d’un enfant malade pour (III₂ × III₃)0,75 pt
Parents : III₂ ♀ × III₃ ♂
Phénotypes : [N] saine × [N] sain
Génotypes : III₂ : XNXn × III₃ : XNY
Gamètes : III₂ : ½ XN et ½ Xn | III₃ : ½ XN et ½ Y
Échiquier de croisement
| ♀ \ ♂ | XN ½ | Y ½ |
|---|---|---|
| XN ½ | XNXN [N] ¼ | XNY [N] ¼ |
| Xn ½ | XNXn [N] ¼ | XnY [n] ¼ |
Probabilité d’avoir un enfant malade = 1/4 (25 %) — uniquement un garçon (XnY)
2 – La Transmission du rachitisme vitamino-résistant
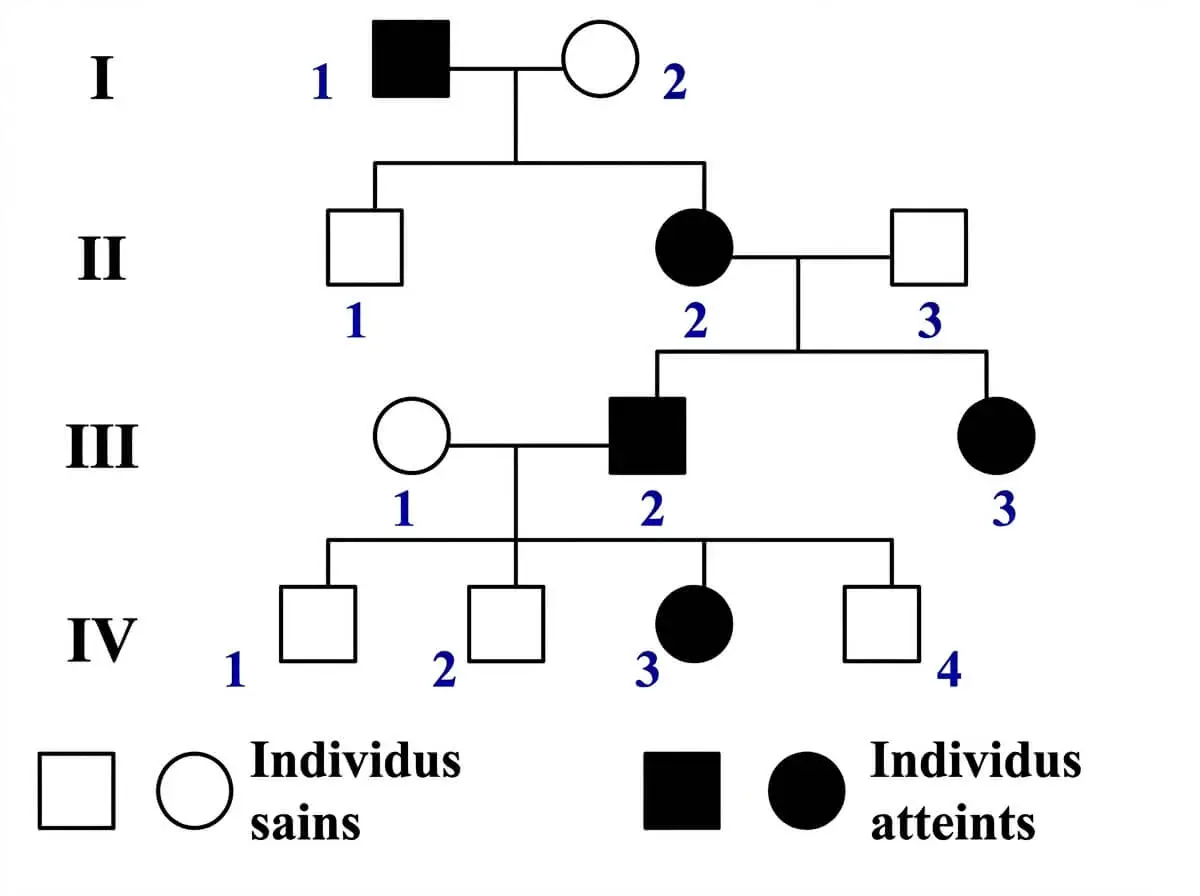
- 1.Déterminez le mode de transmission du rachitisme vitamino-résistant. Justifiez votre réponse.
- 2.Déterminez les génotypes de I₁, I₂, II₂, III₁ et III₂.
- 3.Calculez la probabilité pour que le couple (III₁ × III₂) donne naissance à un enfant atteint. Utilisez l’échiquier de croisement.
Symboles utilisés : A= allèle dominant (maladie) | a = allèle récessif
1.le mode de transmission du rachitisme vitamino-résistant :
I1 est atteint et I2 est saine : leur fille II2 est atteinte → elle a hérité de l’allèle pathologique de son père. Cet allèle s’exprime en une seule copie → il est dominant.
De plus, la maladie apparaît à chaque génération et tout individu atteint possède au moins un parent atteint.
— Le gène n’est pas porté par le chromosome Y : des femmes sont atteintes (II2, III3, IV3).
— Le gène n’est pas porté par un autosome : I1 (père atteint) transmet la maladie à sa fille II2 mais pas à son fils II1, ce qui est cohérent avec une transmission par X (les fils reçoivent Y du père, pas X).
→ Transmission dominante liée au chromosome X.
2.les génotypes de I₁, I₂, II₂, III₁ et III₂ :
I₁ : XAY — père atteint
I₂ : XaXa — mère saine (homozygote), n’a pas transmis la maladie
II₂ : XAXa — fille atteinte, a reçu XAde I₁ et Xade I₂
III₁ : XaXa — femme saine, homozygote (ses fils sains le confirment)
III₂ : XAY — fils atteint de II₂ (a reçu XAde sa mère)
Phénotypes : III₁ ♀ : [a] saine × III₂ ♂ : [A]
Génotypes III₁ : XaXa × III₂ : XAY
Gamètes III₁ : 1 Xa | III₂ : ½ XA et ½ Y
Échiquier de croisement
| ♀ \ ♂ | XA ½ | Y ½ |
|---|---|---|
| Xa 1 | XAXa [A] ½ fille atteinte | XaY [a] ½ garçon sain |
Probabilité d’avoir un enfant atteint = 1/2 (50 %) — uniquement des filles (XAXa)
Probabilité d’avoir un enfant sain = 1/2 (50 %) — uniquement des garçons (XaY)
III – Transmission de maladies héréditaires non liées sexe (Maladies autosomiques) :
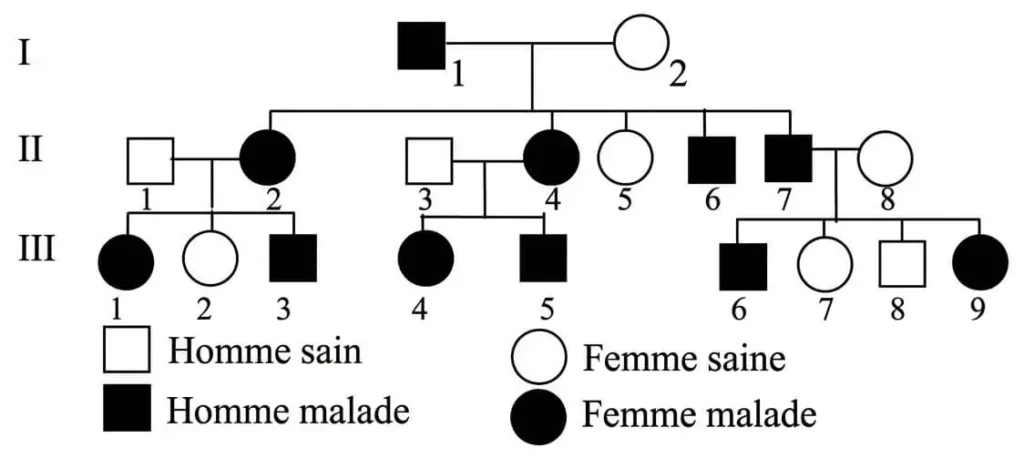
1 – La Transmission de l’albinisme
L’albinisme est une maladie héréditaire caractérisée par l’absence de mélanine, entraînant un déficit de pigmentation de la peau, des cheveux, des poils et des yeux. suivant présente l’arbre généalogique d’une famille touchée par cette affection.
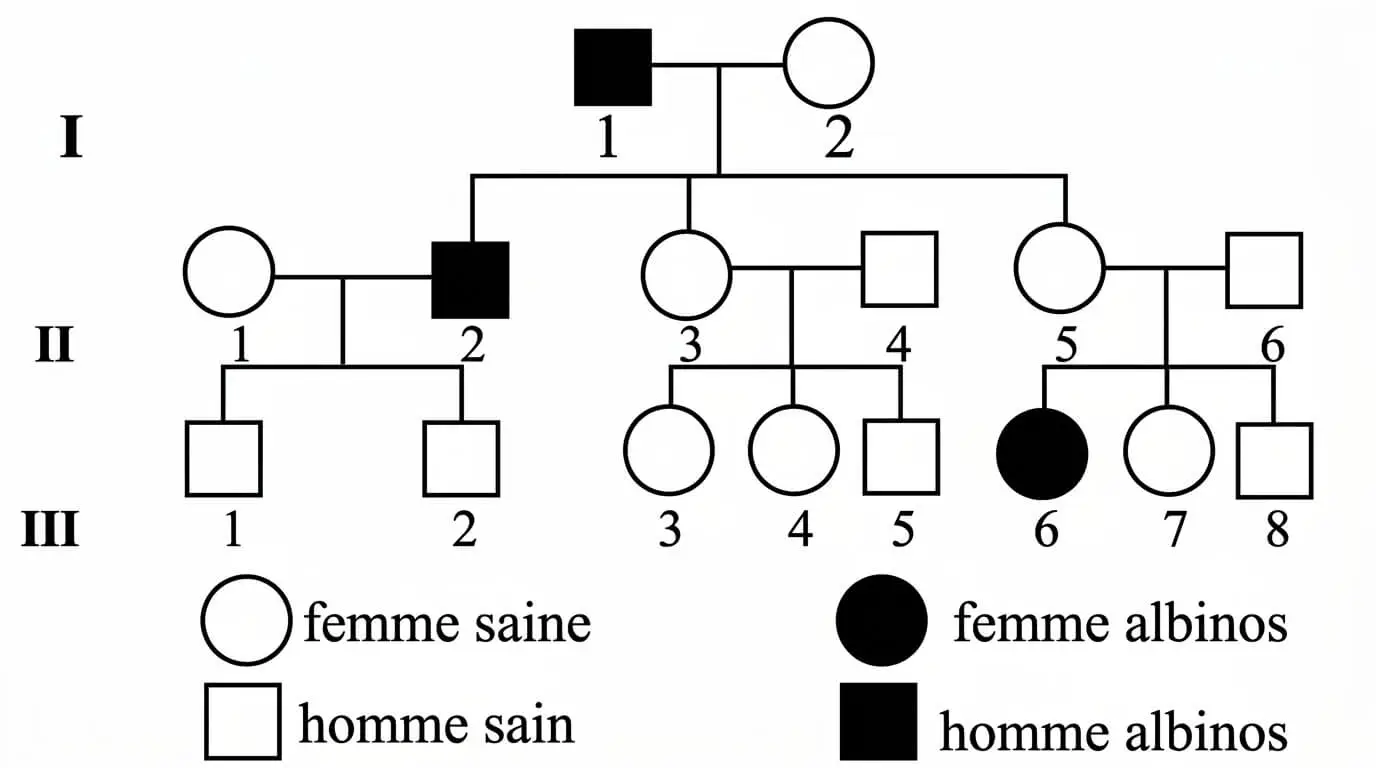
En vous appuyant sur le document :
- 1. Déterminez et justifiez le mode de transmission de l’albinisme.
- 2. Déterminez la probabilité que le couple (II5 × II6) ait un enfant albinos, en justifiant votre réponse à l’aide d’un échiquier de croisement.
(Symboles à utiliser : A pour l’allèle dominant, a pour l’allèle récessif.)
1.Le mode de transmission de l’albinisme:
- L’allèle responsable de l’albinisme est récessif car la fille III6 est albinos et ses parents II5 et II6 sont sains.
- Le gène responsable de l’albinisme est porté par un autosome car le gène n’est pas porté par le chromosome X car la femme III6 est albinos et descend d’un père sain. ou La maladie touche les femmes et les hommes.
2. Probabilité d’un enfant albinos pour le couple (II5 × II6)/ 1 pt
Parents : II5 × II6
Phénotypes : [A] × [A]
Génotypes : A//a × A//a
Gamètes : ½ A/ et ½ a/ — ½ A/ et ½ a/
Échiquier de croisement
| Gamètes | ½ A/ | ½ a/ |
|---|---|---|
| ½ A/ | A//A [A] ¼ | A//a [A] ¼ |
| ½ a/ | A//a [A] ¼ | a//a [a] ¼ |
Probabilité d’avoir un enfant albinos = 1/4 (25 %)
2-La Transmission de la neurofibromatose
Le document suivant présente l’arbre généalogique d’une famille atteinte de neurofibromatose de type 1.

En vous appuyant sur le document 4, et sachant que I2 est homozygote :
- 1. Montrez que l’allèle responsable de la maladie est dominant et autosomique.
- 2. Déterminez la probabilité que le couple (II1 × II2) ait un enfant sain, en justifiant votre réponse à l’aide d’un échiquier de croisement.
(Symboles à utiliser : M pour l’allèle dominant, m pour l’allèle récessif.)
1.
Dominance de l’allèle :
L’enfant malade II4 est issu de la mère I2, qui est saine et homozygote (m//m). Pour que II4 soit malade, il a forcément hérité de l’allèle pathologique de son père I1 → cet allèle s’exprime même en une seule copie : il est donc dominant.
De plus, la maladie est présente à chaque génération et chaque enfant malade possède au moins un parent malade, ce qui confirme la dominance.
Caractère autosomique (non lié au sexe) :
— Le gène n’est pas porté par le chromosome Y : des femmes sont atteintes.
— Le gène n’est pas porté par le chromosome X : une fille saine peut naître d’un père malade, et un garçon sain peut naître d’une mère malade alors que l’allèle responsable est dominant.
→ Le gène est donc porté par un autosome.
2. Probabilité d’un enfant sain pour le couple (II1 × II2) :
Phénotypes : II1 ♂ : [m] sain × II2 ♀ : [M] malade
Génotypes : II1 : m//m II2 : M//m
Gamètes M II1 : 1 m/ | II2 : ½ M/ et ½ m/
Échiquier de croisement
| Gamètes ♀ / ♂ | ½ M/ | ½ m/ |
|---|---|---|
| 1 m/ | M//m ½ [M] | m//m ½ [m] |
Probabilité d’avoir un enfant sain = 1/2 (50 %)
IV-les anomalies chromosomiques et leurs conséquences
Les anomalies chromosomiques regroupent toutes les anomalies de nombre ou de structure d’un (ou plusieurs) chromosome(s) dans un génome, souvent responsables des difficultés cognitives, des malformations congénitales ou d’avortement précoce.
1-anomalies lies aux changements de nombre de chromosomes :
A-Cas des autosomes :
Le syndrome de Down :
le syndrome de Down, est une anomalie chromosomique congénitale. Ses signes cliniques sont très nets, un retard cognitif est observé, associé à des modifications morphologiques particulières. La première étude clinique d’envergure sur la maladie est publiée en 1866 par le médecin britannique, John Langdon Down.
Le document suivant montre le caryotype d’un individu atteint par cette maladie.
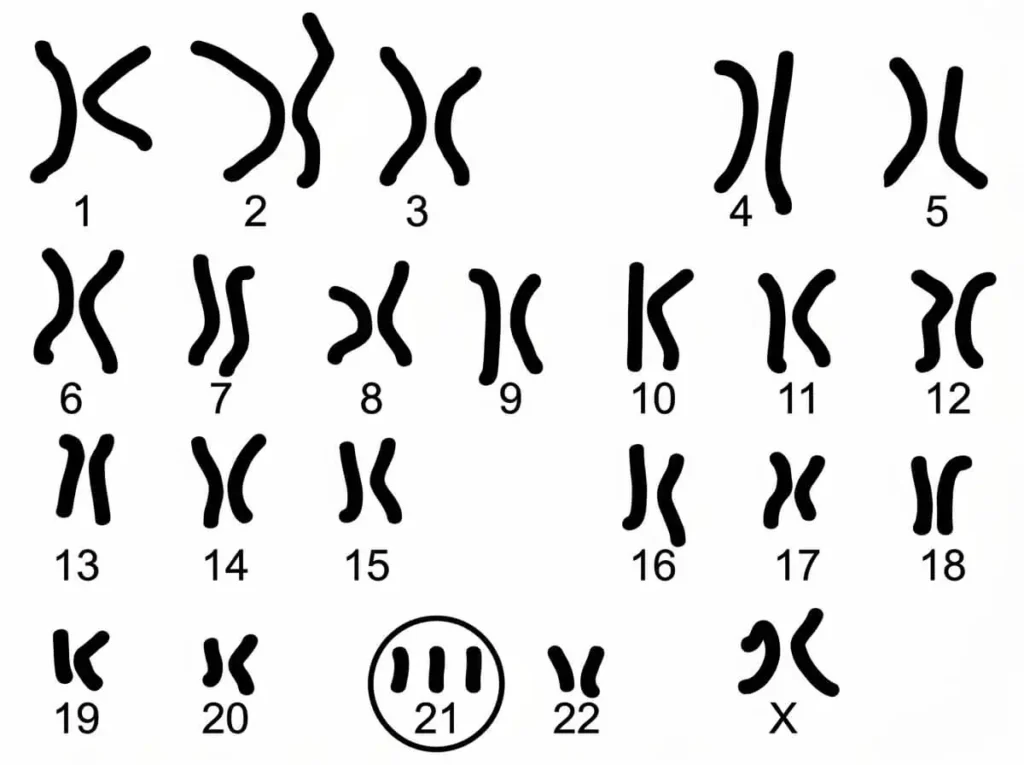
Le caryotype du malade révèle la présence de trois exemplaires du chromosome 21, on parle d’une trisomie 21 .sa formule chromosomique est donc : 2n+1 = 45A+XY
On peut expliquer cette anomalie par la non disjonction des chromosomes 21 au cours de la méiose chez l’un des parents: les 2 chromosomes de la même paire ne se séparent pas et passent ensemble dans la même cellule fille. Cela peut se produire lors de la division réductionnelle (anaphase I) ou bien lors de la division équationnelle (anaphase II). Ainsi se forment des gamètes possédant 2 chromosomes 21. La fécondation d’un gamète anormal par un gamète normal entraîne la formation d’un œuf ayant 3 chromosomes 21.
B-cas des gonosomes :
Syndrome de Turner :
Le syndrome de Turner est une maladie rare d’origine génétique, touchant exclusivement les femmes, et se caractérise par les signes suivants :
Petite taille , absence de caractères sexuels secondaires et stérilité.
De façon plus variable d’autres manifestations, telles que des anomalies du cœur et des reins, ainsi que des particularités au niveau du visage et des membres, peuvent être présentes. Le médecin américain Henry Turner a été le premier à identifier le syndrome en 1938.
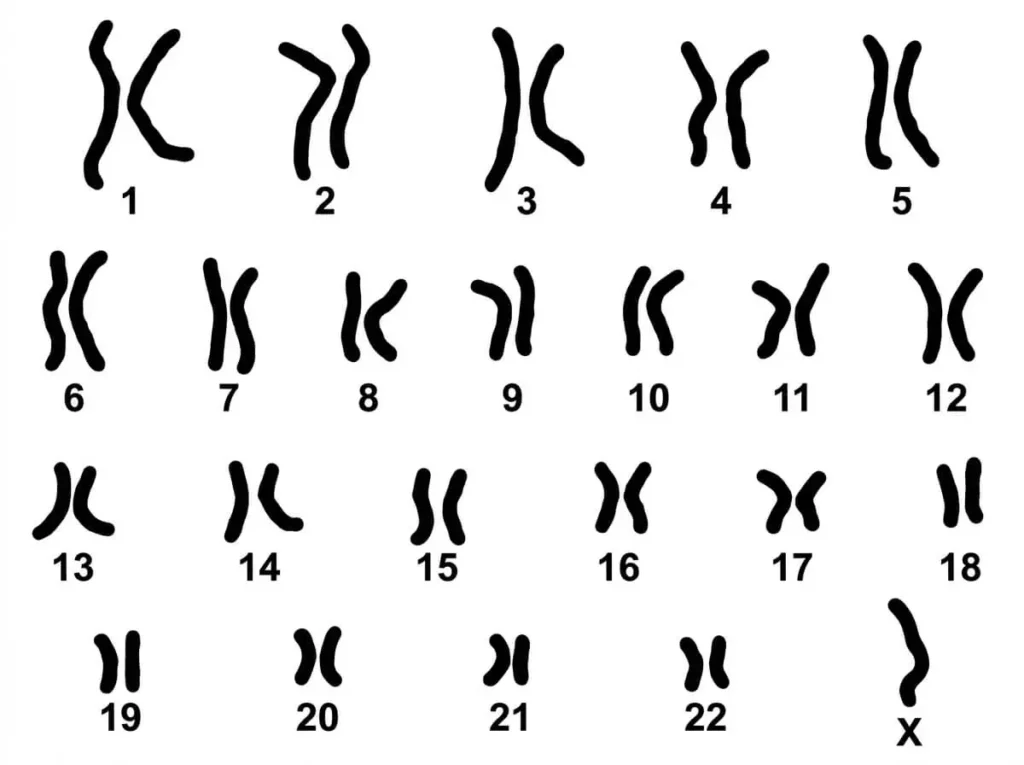
Le document suivant montre le caryotype d’un individu atteint par cette maladie.
1 – On observe que le caryotype du malade révèle la présence d’un seul chromosome sexuel X, on parle d’une monosomie. Sa formule chromosomique est donc : 2n-1 = 44A+X ou 2n-1 = 22AA+X
Syndrome de Klinefelter
C’est une maladie qui affecte les hommes, et se caractérise par la stérilité à cause de l’atrophie des gonades et l’incapacité de produire des gamètes. On observe aussi un faible développement de la pilosité et des facultés intellectuelles. Le syndrome est décrit pour la première fois en 1942 par Harry F. Klinefelter.
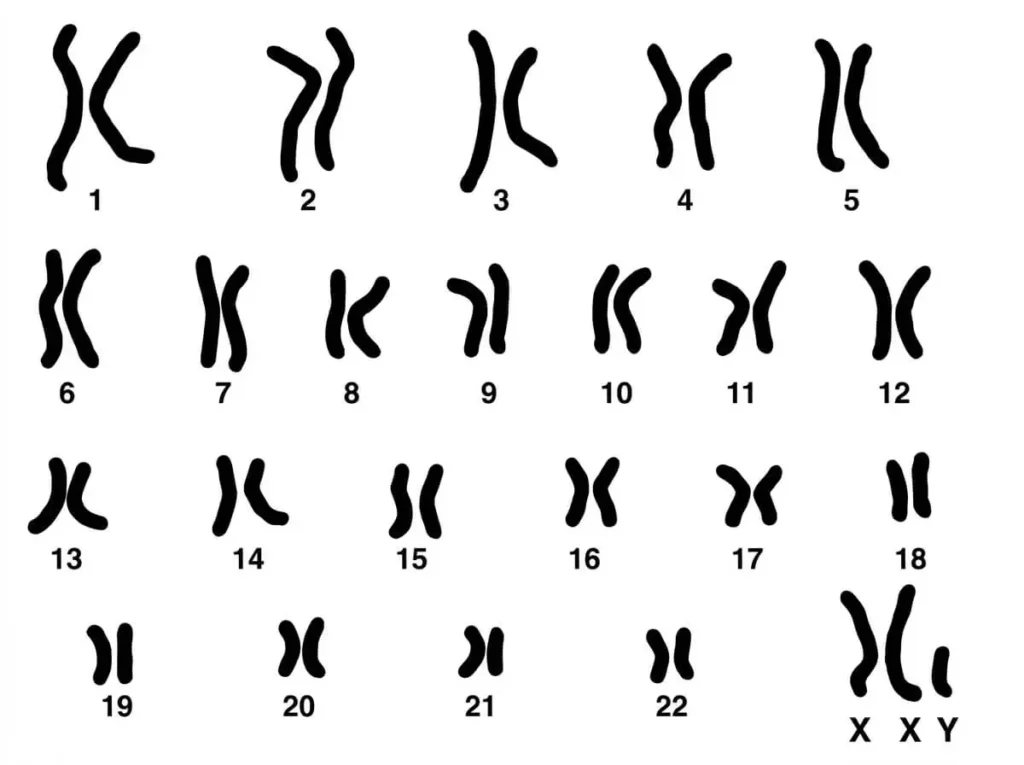
Le document 1 montre le caryotype d’un individu atteint par cette maladie.
Les document 2 et 3 montre les caryotypes de deux autres individus.
1 – On observe que le caryotype du malade révèle la présence d’un trois chromosomes sexuels XXY. Sa formule chromosomique: 2n+1 = 44A+XXY ou 2n+1 = 22AA+XXY
2 – Les anomalies de structure
Maladie de cri de chat
La maladie du cri du chat, ou syndrome de Lejeune est un trouble génétique rare chez l’être humain. Le nom de cette maladie vient du cri monochromatique aigu qui permet le diagnostic de cette maladie. La plupart des décès prématurés ont lieu durant la petite enfance, les survivants ont habituellement un profond retard mental. Jérôme Lejeune est le médecin français ayant décrit cette affection en 1963. Le document suivant montre le caryotype d’un individu atteint par cette maladie.
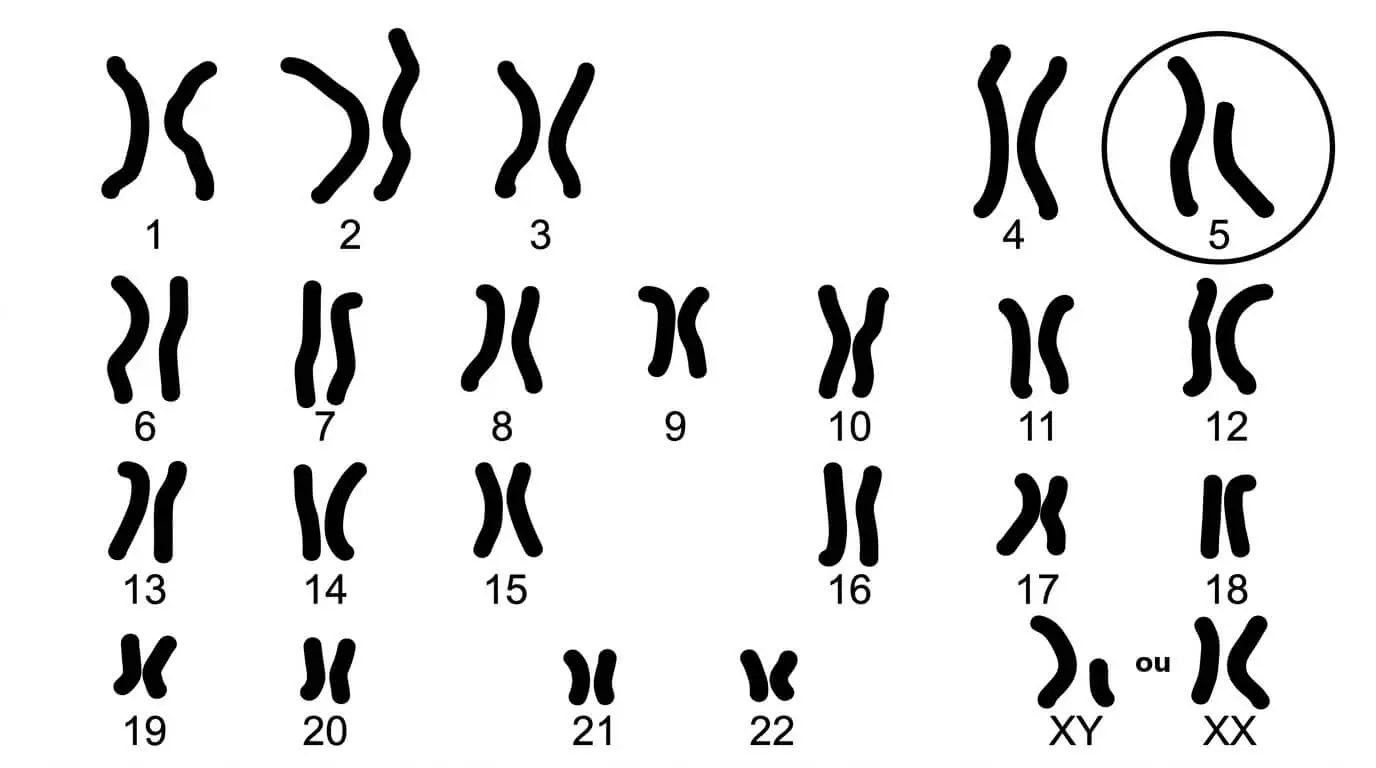
On observe une délétion d’une partie du chromosome 5. La perte d’un fragment du chromosome est accompagnée de perte d’un certain nombre de gènes et donc cet individu aura un phénotype anormal.
Translocations équilibrées
Le document suivant montre le caryotype d’un individu de phenotype normal.
1 – On observe la fusion de l’un des exemplaires du chromosome 21 avec le chromosome 14; on parle d’une translocation.
2 – L’individu a un phénotype normal car il s’agit d’une translocation équilibrée ( il n’y a ni perte ni gain de matériel génétique).
3- ces anomalies résultent de cassures chromosomiques suivies de réparations anormales durant la méiose ou la mitose.
Types d’anomalies structurales :
| Type | Mécanisme | Exemple clinique |
|---|---|---|
| Délétion | Perte d’un fragment de chromosome | Syndrome du cri du chat (délétion 5p) : pleurs caractéristiques, retard mental |
| Duplication | Répétition d’un segment chromosomique | Certaines formes de retard mental |
| Inversion | Rotation à 180° d’un segment | Généralement sans effet phénotypique, problèmes de fertilité |
| Translocation | Transfert d’un segment entre chromosomes non homologues | Certaines leucémies, 5% des trisomies 21 |
Conséquences :
- Perte ou gain de matériel génétique
- Déséquilibre génétique
- Risque de transmission à la descendance
- Fausses couches à répétition
Conclusion : Les anomalies chromosomiques structurales peuvent avoir des conséquences variables selon la quantité et la nature des gènes impliqués.
V – Diagnostic prénatal des maladies génétiques :
1. Définition et Objectifs
Le diagnostic prénatal désigne l’ensemble des examens médicaux pratiqués au cours de la grossesse pour détecter une affection d’une particulière gravité chez l’embryon ou le fœtus.
- Le but : Détecter des anomalies chromosomiques (ex: Trisomie 21) ou géniques (ex: mucoviscidose).
- L’enjeu : Passer d’un risque statistique (probabilité) à une certitude médicale (diagnostic confirmé).
2. L’Échographie : La première étape (Non invasive)
L’échographie est une technique d’imagerie utilisant des ultrasons. C’est l’examen de base car il est sans danger pour la mère et l’enfant.
Elle permet de surveiller :
- La morphologie : Détection de malformations des organes (cœur, membres, cerveau).
- La biométrie : Mesure de la taille du fœtus, du volume de la tête et du diamètre de l’abdomen.
- Les marqueurs spécifiques : Mesure de la clarté nucale (un épaississement peut indiquer une anomalie chromosomique).
- L’environnement : État du placenta et volume du liquide amniotique.
3. Les Techniques de Prélèvement (Invasives)
Si une anomalie est suspectée, le médecin doit prélever des tissus appartenant au fœtus pour les analyser.
| Technique | Période | Nature du prélèvement |
| Choriocentèse | Dès la 8ème semaine | Villosités choriales (futur placenta). |
| Amniocentèse | Dès la 15ème semaine | Liquide amniotique (contenant des cellules fœtales). |
| Cordocentèse | Dès la 17ème semaine | Sang fœtal prélevé dans la veine du cordon ombilical. |
4. Les Analyses de Laboratoire
Une fois les cellules récupérées, trois types de recherches peuvent être menées :
- L’établissement du caryotype : On observe le nombre et la structure des chromosomes pour détecter des aberrations chromosomiques.
- L’analyse de l’ADN : Utilisation de sondes moléculaires pour identifier une mutation précise sur un gène (anomalies géniques).
- Les examens biochimiques : Utilisation de l’électrophorèse pour détecter des protéines anormales ou des troubles du métabolisme.
6. Le Conseil Génétique
Le conseil génétique est une consultation médicale spécialisée visant à informer les couples sur les risques de maladies héréditaires.
A. Les principales indications
Certaines situations rendent la consultation en génétique particulièrement recommandée :
| Situation | Justification |
|---|---|
| Antécédents familiaux de maladie génétique | Risque de transmission |
| Âge maternel ≥ 38 ans | Risque accru d’anomalies chromosomiques |
| Consanguinité | Risque accru de maladies récessives |
| Fausses couches à répétition | Possibles anomalies chromosomiques |
| Exposition à des agents tératogènes | Risque malformatif |
| Naissance antérieure d’un enfant atteint | Risque de récurrence |
Démarche du conseil génétique :
- Établissement de l’arbre généalogique familial
- Identification du mode de transmission
- Calcul des risques pour la descendance
- Information sur les options disponibles
- Accompagnement dans la prise de décision
Conclusion : Le diagnostic prénatal et le conseil génétique constituent des outils essentiels pour la prévention, le dépistage et la prise en charge des maladies génétiques. Ils permettent aux couples à risque de faire des choix éclairé
⚡Révision Express : Le Quiz de 2 minutes
Pas le temps de tout relire ? Va à l’essentiel avec notre test rapide. Score et correction immédiate sans inscription.
